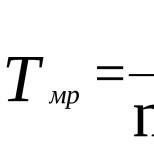Секретное горючее: Пища богов. Агрегат-заправщик РБ жидким кислородом снят с колес и установлен на фундаменте
В таблицах представлена массовая удельная теплота сгорания топлива (жидкого, твердого и газообразного) и некоторых других горючих материалов. Рассмотрено такое топливо, как: уголь, дрова, кокс, торф, керосин, нефть, спирт, бензин, природный газ и т. д.
Перечень таблиц:
При экзотермической реакции окисления топлива его химическая энергия переходит в тепловую с выделением определенного количества теплоты. Образующуюся тепловую энергию принято называть теплотой сгорания топлива. Она зависит от его химического состава, влажности и является основным . Теплота сгорания топлива, отнесенная на 1 кг массы или 1 м 3 объема образует массовую или объемную удельную теплоты сгорания.
Удельной теплотой сгорания топлива называется количество теплоты, выделяемое при полном сгорании единицы массы или объема твердого, жидкого или газообразного топлива. В Международной системе единиц эта величина измеряется в Дж/кг или Дж/м 3 .
Удельную теплоту сгорания топлива можно определить экспериментально или вычислить аналитически. Экспериментальные методы определения теплотворной способности основаны на практическом измерении количества теплоты, выделившейся при горении топлива, например в калориметре с термостатом и бомбой для сжигания. Для топлива с известным химическим составом удельную теплоту сгорания можно определить по формуле Менделеева .
Различают высшую и низшую удельные теплоты сгорания. Высшая теплота сгорания равна максимальному количеству теплоты, выделяемому при полном сгорании топлива, с учетом тепла затраченного на испарение влаги, содержащейся в топливе. Низшая теплота сгорания меньше значения высшей на величину теплоты конденсации , который образуется из влаги топлива и водорода органической массы, превращающегося при горении в воду.
Для определения показателей качества топлива, а также в теплотехнических расчетах обычно используют низшую удельную теплоту сгорания , которая является важнейшей тепловой и эксплуатационной характеристикой топлива и приведена в таблицах ниже.
Удельная теплота сгорания твердого топлива (угля, дров, торфа, кокса)
В таблице представлены значения удельной теплоты сгорания сухого твердого топлива в размерности МДж/кг. Топливо в таблице расположено по названию в алфавитном порядке.
Наибольшей теплотворной способностью из рассмотренных твердых видов топлива обладает коксующийся уголь — его удельная теплота сгорания равна 36,3 МДж/кг (или в единицах СИ 36,3·10 6 Дж/кг). Кроме того высокая теплота сгорания свойственна каменному углю, антрациту, древесному углю и углю бурому.
К топливам с низкой энергоэффективностью можно отнести древесину, дрова, порох, фрезторф, горючие сланцы. Например, удельная теплота сгорания дров составляет 8,4…12,5, а пороха — всего 3,8 МДж/кг.
| Топливо | |
|---|---|
| Антрацит | 26,8…34,8 |
| Древесные гранулы (пиллеты) | 18,5 |
| Дрова сухие | 8,4…11 |
| Дрова березовые сухие | 12,5 |
| Кокс газовый | 26,9 |
| Кокс доменный | 30,4 |
| Полукокс | 27,3 |
| Порох | 3,8 |
| Сланец | 4,6…9 |
| Сланцы горючие | 5,9…15 |
| Твердое ракетное топливо | 4,2…10,5 |
| Торф | 16,3 |
| Торф волокнистый | 21,8 |
| Торф фрезерный | 8,1…10,5 |
| Торфяная крошка | 10,8 |
| Уголь бурый | 13…25 |
| Уголь бурый (брикеты) | 20,2 |
| Уголь бурый (пыль) | 25 |
| Уголь донецкий | 19,7…24 |
| Уголь древесный | 31,5…34,4 |
| Уголь каменный | 27 |
| Уголь коксующийся | 36,3 |
| Уголь кузнецкий | 22,8…25,1 |
| Уголь челябинский | 12,8 |
| Уголь экибастузский | 16,7 |
| Фрезторф | 8,1 |
| Шлак | 27,5 |
Удельная теплота сгорания жидкого топлива (спирта, бензина, керосина, нефти)
Приведена таблица удельной теплоты сгорания жидкого топлива и некоторых других органических жидкостей. Следует отметить, что высоким тепловыделением при сгорании отличаются такие топлива, как: бензин, дизельное топливо и нефть.
Удельная теплота сгорания спирта и ацетона существенно ниже традиционных моторных топлив. Кроме того, относительно низким значением теплоты сгорания обладает жидкое ракетное топливо и — при полном сгорании 1 кг этих углеводородов выделится количество теплоты, равное 9,2 и 13,3 МДж, соответственно.
| Топливо | Удельная теплота сгорания, МДж/кг |
|---|---|
| Ацетон | 31,4 |
| Бензин А-72 (ГОСТ 2084-67) | 44,2 |
| Бензин авиационный Б-70 (ГОСТ 1012-72) | 44,1 |
| Бензин АИ-93 (ГОСТ 2084-67) | 43,6 |
| Бензол | 40,6 |
| Дизельное топливо зимнее (ГОСТ 305-73) | 43,6 |
| Дизельное топливо летнее (ГОСТ 305-73) | 43,4 |
| Жидкое ракетное топливо (керосин + жидкий кислород) | 9,2 |
| Керосин авиационный | 42,9 |
| Керосин осветительный (ГОСТ 4753-68) | 43,7 |
| Ксилол | 43,2 |
| Мазут высокосернистый | 39 |
| Мазут малосернистый | 40,5 |
| Мазут низкосернистый | 41,7 |
| Мазут сернистый | 39,6 |
| Метиловый спирт (метанол) | 21,1 |
| н-Бутиловый спирт | 36,8 |
| Нефть | 43,5…46 |
| Нефть метановая | 21,5 |
| Толуол | 40,9 |
| Уайт-спирит (ГОСТ 313452) | 44 |
| Этиленгликоль | 13,3 |
| Этиловый спирт (этанол) | 30,6 |
Удельная теплота сгорания газообразного топлива и горючих газов
Представлена таблица удельной теплоты сгорания газообразного топлива и некоторых других горючих газов в размерности МДж/кг. Из рассмотренных газов наибольшей массовой удельной теплотой сгорания отличается . При полном сгорании одного килограмма этого газа выделится 119,83 МДж тепла. Также высокой теплотворной способностью обладает такое топливо, как природный газ — удельная теплота сгорания природного газа равна 41…49 МДж/кг (у чистого 50 МДж/кг).
| Топливо | Удельная теплота сгорания, МДж/кг |
|---|---|
| 1-Бутен | 45,3 |
| Аммиак | 18,6 |
| Ацетилен | 48,3 |
| Водород | 119,83 |
| Водород, смесь с метаном (50% H 2 и 50% CH 4 по массе) | 85 |
| Водород, смесь с метаном и оксидом углерода (33-33-33% по массе) | 60 |
| Водород, смесь с оксидом углерода (50% H 2 50% CO 2 по массе) | 65 |
| Газ доменных печей | 3 |
| Газ коксовых печей | 38,5 |
| Газ сжиженный углеводородный СУГ (пропан-бутан) | 43,8 |
| Изобутан | 45,6 |
| Метан | 50 |
| н-Бутан | 45,7 |
| н-Гексан | 45,1 |
| н-Пентан | 45,4 |
| Попутный газ | 40,6…43 |
| Природный газ | 41…49 |
| Пропадиен | 46,3 |
| Пропан | 46,3 |
| Пропилен | 45,8 |
| Пропилен, смесь с водородом и окисью углерода (90%-9%-1% по массе) | 52 |
| Этан | 47,5 |
| Этилен | 47,2 |
Удельная теплота сгорания некоторых горючих материалов
Приведена таблица удельной теплоты сгорания некоторых горючих материалов ( , древесина, бумага, пластик, солома, резина и т. д.). Следует отметить материалы с высоким тепловыделением при сгорании. К таким материалам можно отнести: каучук различных типов, пенополистирол (пенопласт), полипропилен и полиэтилен.
| Топливо | Удельная теплота сгорания, МДж/кг |
|---|---|
| Бумага | 17,6 |
| Дерматин | 21,5 |
| Древесина (бруски влажностью 14 %) | 13,8 |
| Древесина в штабелях | 16,6 |
| Древесина дубовая | 19,9 |
| Древесина еловая | 20,3 |
| Древесина зеленая | 6,3 |
| Древесина сосновая | 20,9 |
| Капрон | 31,1 |
| Карболитовые изделия | 26,9 |
| Картон | 16,5 |
| Каучук бутадиенстирольный СКС-30АР | 43,9 |
| Каучук натуральный | 44,8 |
| Каучук синтетический | 40,2 |
| Каучук СКС | 43,9 |
| Каучук хлоропреновый | 28 |
| Линолеум поливинилхлоридный | 14,3 |
| Линолеум поливинилхлоридный двухслойный | 17,9 |
| Линолеум поливинилхлоридный на войлочной основе | 16,6 |
| Линолеум поливинилхлоридный на теплой основе | 17,6 |
| Линолеум поливинилхлоридный на тканевой основе | 20,3 |
| Линолеум резиновый (релин) | 27,2 |
| Парафин твердый | 11,2 |
| Пенопласт ПХВ-1 | 19,5 |
| Пенопласт ФС-7 | 24,4 |
| Пенопласт ФФ | 31,4 |
| Пенополистирол ПСБ-С | 41,6 |
| Пенополиуретан | 24,3 |
| Плита древесноволокнистая | 20,9 |
| Поливинилхлорид (ПВХ) | 20,7 |
| Поликарбонат | 31 |
| Полипропилен | 45,7 |
| Полистирол | 39 |
| Полиэтилен высокого давления | 47 |
| Полиэтилен низкого давления | 46,7 |
| Резина | 33,5 |
| Рубероид | 29,5 |
| Сажа канальная | 28,3 |
| Сено | 16,7 |
| Солома | 17 |
| Стекло органическое (оргстекло) | 27,7 |
| Текстолит | 20,9 |
| Толь | 16 |
| Тротил | 15 |
| Хлопок | 17,5 |
| Целлюлоза | 16,4 |
| Шерсть и шерстяные волокна | 23,1 |
Источники:
- ГОСТ 147-2013 Топливо твердое минеральное. Определение высшей теплоты сгорания и расчет низшей теплоты сгорания.
- ГОСТ 21261-91 Нефтепродукты. Метод определения высшей теплоты сгорания и вычисление низшей теплоты сгорания.
- ГОСТ 22667-82 Газы горючие природные. Расчетный метод определения теплоты сгорания, относительной плотности и числа Воббе.
- ГОСТ 31369-2008 Газ природный. Вычисление теплоты сгорания, плотности, относительной плотности и числа Воббе на основе компонентного состава.
- Земский Г. Т. Огнеопасные свойства неорганических и органических материалов: справочник М.: ВНИИПО, 2016 — 970 с.
Всем известно, что в нашей жизни огромную роль играет использование топлива. Топливо применяют практически в любой отрасли современной промышленности. Особенно часто применяется топливо, полученное из нефти: бензин, керосин, соляр и другие. Также применяют горючие газы (метан и другие).
Откуда берется энергия у топлива
Известно, что молекулы состоят из атомов . Для того, чтобы разделить какую либо молекулу (например, молекулу воды) на составляющие её атомы, требуется затратить энергию (на преодоление сил притяжения атомов). Опыты показывают, что при соединении атомов в молекулу (это и происходит при сжигании топлива) энергия, напротив, выделяется.
Как известно, существует ещё и ядерное топливо, но мы не будем здесь говорить о нём.
При сгорании топлива выделяется энергия. Чаще всего это тепловая энергия . Опыты показывают, что количество выделившейся энергии прямо пропорционально количеству сгоревшего топлива.
Удельная теплота сгорания
Для расчёта этой энергии используют физическую величину, называемую удельная теплота сгорания топлива. Удельная теплота сгорания топлива показывает, какая энергия выделяется при сгорании единичной массы топлива.
Её обозначают латинской буквой q. В системе СИ единица измерения этой величины Дж/кг. Отметим, что каждое топливо имеет собственную удельную теплоту сгорания. Эта величина измерена практически для всех видов топлива и при решении задач определяется по таблицам.
Например, удельная теплота сгорания бензина 46 000 000 Дж/кг, керосина такая же, этилового спирта 27 000 000 Дж/кг. Нетрудно понять, что энергия, выделившаяся при сгорании топлива, равна произведению массы этого топлива и удельной теплоты сгорания топлива:
Рассмотрим примеры
Рассмотрим пример. 10 граммов этилового спирта сгорело в спиртовке за 10 минут. Найдите мощность спиртовки.
Решение. Найдём количество теплоты, выделившееся при сгорании спирта:
Q = q*m; Q = 27 000 000 Дж/кг * 10 г = 27 000 000 Дж/кг * 0,01 кг = 270 000 Дж.
Найдём мощность спиртовки:
N = Q / t = 270 000 Дж / 10 мин = 270 000 Дж / 600 с = 450 Вт.
Рассмотрим более сложный пример. Алюминиевую кастрюлю массой m1, заполненную водой массой m2, нагрели с помощью примуса от температуры t1 до температуры t2 (00С < t1 < t2
Решение.
Найдём количество теплоты, полученное алюминием:
Q1 = c1 * m1 * (t1 t2);
найдём количество теплоты, полученное водой:
Q2 = c2 * m2 * (t1 t2);
найдём количество теплоты, полученное кастрюлей с водой:
найдём количество теплоты, отданное сгоревшим бензином:
Q4 = Q3 / k * 100 = (Q1 + Q2) / k * 100 =
(c1 * m1 * (t1 t2) + c2 * m2 * (t1 t2)) / k * 100;
Энергоемкость топлив
Важнейшей характеристикой топлива является его энергоемкость, или теплота сгорания. Под энергоемкостью (или теплотой сгорания) следует понимать количество теплоты, выделившейся при полном сгорании единицы массы или объема топлива и замеренной при постоянных давлении и температуре (обычно при 25 °С).
В технике пользуются значением низшей теплоты сгорания 1 кг (весовой) или 1 л (объемной) топлива. Низшая теплота сгорания топлива (расчетная) получается уменьшением значения высшей теплоты сгорания (экспериментальной) на количество тепла, затраченного для испарения некоторых продуктов сгорания, которые при нормальной температуре являются жидкостями. В основном - это вода, которая выводится из двигателя с продуктами сгорания в парообразном состоянии. При этом исходят из того, что тепло образования водяных паров теряется безвозвратно.
В том случае, когда среди продуктов сгорания топлива не оказывается соединений, конденсирующихся при нормальной температуре, например при сжигании СО в СО 2 , высшая и низшая теплоты сгорания равны.
Для работы современных карбюраторных, дизельных и ракетных двигателей важно знать также теплоту сгорания рабочей смеси, состоящей из горючего и окислителя, в количестве, достаточном для полного сгорания горючего. При этом наибольшая теплота сгорания будет у рабочей.смеси, в которой стехиометрическое соотношение топливо: окислитель? равно 1.
Значение низшей теплоты сгорания рабочих смесей, состоящих из паров углеводородов с воздухом, приближается к 667- 674 ккал/кг.
Углеводородные топлива характеризуются высокой теплотой сгорания. Продуктами их полного сгорания являются, главным образом, двуокись углерода и вода. Лишь водород, бериллий и бор имеют большие теплоты сгорания, чем углеводороды. Однако при их использовании в качестве топлив возникают весьма сложные проблемы, которые здесь не рассматриваются. По эксплуатационным свойствам углеводороды как топлива отличаются значительными преимуществами.
Теплоту сгорания определяют сжиганием навески топлива в калориметрической бомбе, заполненной кислородом под давлением. Метод этот сложен, и для его осуществления требуются специальные условия.
Для определения теплоты сгорания при помощи расчетов широко пользуются эмпирическими формулами, точность которых составляет ±2-3%.
В основу эмпирических расчетных формул, составленных различными авторами, положены следующие данные.
1. Элементарный состав топлива. В этом случае исходят из того, что теплота сгорания топлива равна сумме теплот сгорания отдельных элементов его составляющих.
2. Количество кислорода (воздуха), необходимого для сгорания топлива. В основу эмпирических формул положено количество кислорода, необходимое для полного сгорания элементов, составляющих топливо. Наибольшей точностью из формул этого типа отличается формула Коновалова:
Q н = 3050 К
Где Q н - низшая теплота сгорания топлива, ккал/кг; К - количество кислорода, необходимого для сгорания единицы массы топлива, рассчитываемое по формуле:
где С, Н, О - содержание углерода, водорода и кислорода в топливе, вес. %.
3. Теплота образования. Эмпирические формулы основаны на законе Гесса, из которого следует, что теплота сгорания топлива соответствует разности между теплотой образования сжигаемого топлива и суммой теплот образования конечных продуктов его сгорания (воды, двуокиси углерода и др.).
4. Физико-химические характеристики топлива. Для углеводородных жидких топлив, состоящих в основном из двух элементов-углерода и водорода, устанавливается определенная зависимость между отношением этих элементов, температурой их выкипания, анилиновой точкой, плотностью, строением углеводородов и другими физико-химическими показателями, с одной стороны, и теплотой сгорания - с другой.
Для углеводородных топлив, имеющих плотность от 0,510 до 0,990, весовая теплота сгорания может быть определена с точностью до 3-5% (для фракций алканового основания до 1 - 1,5%) по формулам Крагоэ:

где?-плотность топлива при 15°С; Q в - высшая теплота сгорания, ккал/кг; О н - низшая теплота сгорания, ккал/кг.
Установлено, что при использовании этой формулы наименьшая погрешность составляет 40 ккал/кг; для смесси ароматических углеводородов с алканами наибольшая погрешность достигает 400-530 ккал/кг.
Лаврентьев предложил эмпирическую формулу для расчета низшей весовой теплоты сгорания по значению показателя преломления:
Для товарных реактивных топлив максимальное отклонение вычисленных данных, определенных экспериментально, составляет ±95 ккал/кг при среднем отклонении ±1,4 ккал/кг. Неудовлетворительные результаты получаются для узких нефтяных фракций, индивидуальных углеводородов, особенно ароматических углеводородов, для которых величина отклонения превосходит 400 ккал/кг.
Более точные результаты (отклонение ±20-25 ккал/кг), в том числе для ароматических углеводородов, дает формула, в которой используется показатель преломления и анилиновая точка:
где t A - анилиновая точка, °С.
Для среднедистиллятных нефтяных топлив можно достаточно точно рассчитать низшую весовую теплоту сгорания, зная содержание водорода, по формуле:
где Н - содержание водорода, вес. %.
Многие авторы считают, что наибольшая точность достигается при использовании расчетных формул, в которых представлена зависимость между теплотой сгорания, плотностью и анилиновой точкой среднедистиллятных топлив. Результаты расчета при использовании такой зависимости приняты во всех спецификациях США и других стран на реактивные топлива наравне со значениями, определенными экспериментально. Для керосинов отклонения от экспериментальных данных составляют 12- 14 ккал/кг, максимальные отклонения ± 45 ккал/кг. Небольшое содержание олефинов в керосинах существенно не влияет на результаты. Для алкилатов и индивидуальных углеводородов, кипящих в пределах керосиновых фракций, этот метод мало пригоден.
В спецификациях на реактивные топлива приводится коэффициент теплопроводности, представляющий собой произведение плотности, выраженной в °АРI (АSТМ D 287-55), и анилиновой точки в °F (АSТМ D 611-55Т), изменяющейся с теплотой сгорания топлива по линейной зависимости. В результате проверки этого метода на многочисленных образцах реактивных топлив нашей страны была предложена формула:
где К - коэффициент теплотворности топлива, численно равный произведению плотности топлива в °АРI и анилиновой точки в °F. Плотность определяется при 15,6 °С по ГОСТ 3900-47, а анилиновая точка - методом равных объемов (ОСТ 17872 М. И. 20К-40). Для получения плотности в °АРI, а анилиновой точки в °F пользуются переводными таблицами, приведенными в работах.
При использовании этой формулы можно получить результаты с точностью до 0,12% и максимальным отклонением 0,43% для нефтепродуктов плотностью? 5.16 15.6 =0,8448-0,7585 (36- 55°АРI), имеющих анилиновую точку 51-78,3 °С (124-173°F) и коэффициенты теплотворности в пределах от 4414 до 8969.
Некоторая ошибка получается при наличии в топливе серы. Так, при 1 % серы значение теплоты сгорания для керосина может быть завышено приблизительно на 60 ккал/кг. Поэтому для расчета низшей теплоты сгорания предлагается формула, учитывающая содержание серы:
где Q н -теплота сгорания топлива, содержащего серу, ккал/кг;
Q н - теплота сгорания, рассчитанная для топлива по анилиновой точке и плотности без учета содержания серы, ккал/кг; %S- содержание серы в топливе, вес. %.

Зная плотность? 15.6 15.6 и вязкость топлива (в сст) при 37,8 °С, по номограмме (рис. 18) можно определить анилиновую точку в °С, а затем перевести в °F. Отклонения для керосинов от данных, полученных стандартным методом, не превышают ± 2%.
Ниже приведены коэффициенты теплотворности и значения низшей весовой теплоты сгорания для различных реактивных топлив, рассчитанные по формуле.
Для упрощения расчетов предложены номограммы, составленные на основании зависимости между физико-химическими и энергетическими характеристиками нефтяных фракций. Ниже в качестве примера представлена одна из подобных номограмм,

построенная на основе зависимости между плотностью, молекулярным весом, псевдокритическим давлением, анилиновой точкой, средней температурой кипения, теплотой испарения и высшей теплотой сгорания для нефтяных фракций (рис. 19).

Зная две какие либо характеристики из названных, можно по номограмме определить остальные. При работе с номограммой среднюю температуру кипения фракции можно принять равной температуре выкипания 50 объемн. % этой фракции в условиях стандартной разгонки.
Поскольку на номограмме приведены значения высшей теплоты сгорания, значение низшей теплоты сгорания можно рассчитать по формуле:
где К - содержание в топливе воды, вес. %.
Отклонения данных, полученных по номограмме, от фактических данных составляют 1%.

На рис. 20 приведена номограмма зависимости между низшей объемной теплотой сгорания, плотностью, вязкостью и средней температурой выкипания дизельных топлив.
По такой номограмме при помощи известных характеристик можно легко определить объемную теплоту сгорания дизельных топлив.
Теплота сгорания зависит от элементарного состава углеводородов топлива, что подтверждается следующими данными:

Весовая теплота сгорания водорода в 3,5 раза больше весовой теплоты сгорания углерода. Чем выше содержание водорода, тем выше теплота сгорания углеводородного топлива.
Для алканов среднедистиллятных фракций содержание углерода изменяется незначительно - в пределах 84-85%, для цикланов эта величина постоянна и составляет приблизительно 85,75%, для ароматических углеводородов она изменяется в широких пределах - от 91 до 87,5% и зависит от длины боковых цепей.

Весовые теплоты сгорания топлива изменяются в соответствии с содержанием углерода: для алканов и цикланов незначительно, а для ароматических углеводородов с числом углеродных атомов от 6 до 20 - до 700 ккал (рис. 21). Плотность ? 4 20 углеводородов, составляющих товарные топлива и выкипающих в пределах 80-300°С, изменяется следующим образом :
Плотность в пределах одного класса углеводородов изменяется значительно. Она определяется не только молекулярным весом, но и структурой углеводородов. Вследствие этого объемные теплоты сгорания углеводородов существенно различаются.
Для углеводородов промышленных фракций, однотипных по строению и выкипающих в пределах 100-300°С, разница между максимальной и минимальной величинами весовой теплоты сгорания составляет от 30 до 350 ккал/кг, объемной- от 30 до 1100 ккол/л. Особенно велика разница объемной теплоты сгорания у цикланов - 700-1100 ккал/л (табл. 19).

Объемную теплоту сгорания можно значительно увеличить, одновременно сохраняя на достаточно высоком уровне весовую теплоту сгорания, вовлечением в состав топлив цикланов определенного строения.
Нефтяные топлива характеризуются теплотой сгорания, близкой к верхнему возможному пределу. Однако для дальнейшего увеличения теплоты сгорания углеводородных топлив остаются некоторые резервы. Все больше синтезируется, а также выделяется из нефти углеводородов такого строения, теплоты сгорания (весовые и объемные) которых существенно превышают теплоты сгорания товарных нефтяных фракций. На основе таких углеводородов предлагаются новые композиции высокоэнергетических топлив, столь необходимых для реактивных и ракетных двигателей.
Применение топлива с повышенной теплотой сгорания для карбюраторных и дизельных двигателей приведет к снижению его удельного расхода (поскольку теплота сгорания рабочей смеси должна быть постоянной); к уменьшению объема топливных баков при том же радиусе действия машин; к некоторому изменению сечения жиклеров в соответствии с количеством поступающего топлива. Мощность карбюраторных и дизельных двигателей не зависит от теплоты сгорания топлива и, следовательно, остается неизменной.
Для реактивных и ракетных двигателей, в которых сила тяги создается только за счет сил реакции газов, вытекающих из сопла, теплота сгорания топлива играет большую роль. Сила тяги воздушно-реактивного двигателя представляет равнодействующую сил воздушного и газового потоков, оказывающую влияние на элементы "Проточной части и наружной поверхности двигателя. Она прямо пропорциональна количеству воздуха, проходящего через реактивный двигатель, и скорости истечения газов через его сопло. Весовой расход топлива составляет 1,5-2% от весового расхода воздуха. Топливо, сгорая, нагревает воздух и тем самым увеличивает его кинетическую энергию, расходуемую на полезную работу и компенсацию потерь. Поэтому чем выше теплота сгорания топлива, тем большую полезную работу сможет дать двигатель.
Увеличение теплоты сгорания топлива приведет к увеличению объема газов, проходящих через двигатель, и, следовательно, к увеличению скорости их истечения, что повысит к. п. д. двигателя. Авиационные топлива, выделяющие при сгорании большее количество тепла, позволяют увеличить дальность полета или грузоподъемность самолета. О зависимости между энергоемкостью авиационного реактивного топлива и дальностью полета самолета можно судить по формуле Брегэ:

где К - дальность оолета; Q н - весовая низшая теплота сгорания топлива; ? - суммарный к. п. д. двигателя; L / D - отношение подъемной силы к лобовому сопротивлению; W 0 - вес самолета при старте; W f - вес залитого в баки самолета топлива.
Из приведенной формулы следует, что дальность полета самолета изменяется (прямо пропорционально теплоте, выделяющейся при сгорании топлива. Таким образом, при постоянном весе топлива повышение его весовой теплоты сгорания позволит в реактивном двигателе не только достичь преимуществ, указанных для карбюраторных двигателей, но и увеличить мощность двигателя, скорость м дальность полета самолета или уменьшить удельный расход топлива.
Увеличение объемной теплоты сгорания топлива, связанное с обязательным возрастанием его плотности, даст преимущества лишь в том случае, если прирост теплоты сгорания превзойдет потери энергии, которую необходимо будет дополнительно затратить вследствие увеличения полетного веса самолета, загруженного таким же объемом топлива, но имеющего большую плотность. Критерием энергетической оценки топлива будет являться удельная теплота сгорания загруженного топлива, отнесенная к единице полетного веса летательного аппарата.
Весьма желательно равенство значений весовой и объемной теплоты сгорания топлив; к такому равенству можно приблизиться, увеличивая плотность углеводородной смеси до единицы.
Выполнить это условие пока трудно, хотя методом синтеза удается получить насыщенные углеводороды, плотность которых превышает 0,9 г/см 3 .

На рис. 22 показано влияние теплоты сгорания и плотности топлива на дальность полета самолета при различных высотах. Как видно из рисунка, энергетические преимущества топлива с повышенной плотностью наиболее ощутимы при большой скорости полета (2,5-4 Маха).
При необходимости увеличения дальности полета топливо с большей весовой теплотой сгорания в сравнимых условиях будет обладать (преимуществом перед топливом с большей объемной теплотой сгорания (большей плотностью). На дальних расстояниях при использовании последних будет расходоваться дополнительная энергия на их перевозку.
Для ракетного двигателя значение топлива с высокой теплотой сгорания еще более возрастает. Высота взлета ракетного двигателя увеличивается во столько раз, во сколько увеличивается теплота сгорания топлива. Таким образом, при использовании для ракетных двигателей топлив с более высокой теплотой сгорания достигаются преимущества, указанные для воздушно-ракетных двигателей, и увеличивается высота взлета ракеты.
Исследователи стремятся получить такое углеводородное топливо, которое возможно полнее отвечало бы требованиям реактивных сверхзвуковых и тем более ракетных двигателей. Такие топлива должны характеризоваться высокой весовой и объемной теплотой сгорания при минимальном различии их значений. Кроме того, углеводороды, составляющие топлива, должны обладать удовлетворительными низкотемпературными свойствами, высокой химической стабильностью при повышенных температурах, пределами кипения и др. Предпринимаются попытки получения таких топлив не только на основе соответствующих нефтяных фракций и однотипных по химическому строению групп углеводородов, но и на основе сложного синтеза индивидуальных соединений, хотя этот путь намного дороже. В табл. 20 приведены сведения о некоторых синтезированных для этой цели в США индивидуальных углеводородах по данным патентной литературы, опубликованной в основном в 1964 г.

Как видно из данных табл. 20, осуществлен синтез углеводородов сложных и интересных структур. Исследование их свойств свидетельствует об известных возможностях, обнаруженных на этом пути. Большинство углеводородов являются би- и трицикланами с очень высокой плотностью, а следовательно, высокой объемной теплотой сгорания.
По-видимому, циклановые углеводороды в целом отвечают требованиям, предъявляемым к топливу, ;В большей мере, чем углеводороды иного строения. Можно предвидеть, что изоалка- новые углеводороды определенного строения также окажутся благоприятным материалом для этой цели.
Поскольку для реактивных топлив сверхзвуковых самолетов наиболее подходящим и доступным в настоящее время материалом являются циклановые углеводороды, характеризующиеся достаточно высокой весовой теплотой сгорания и плотностью, значения низшей весовой теплоты сгорания цикланов различного строения при 25°С (в ккал/кг).
Наряду с цикланами большое внимание заслуживают с точки зрения использования в качестве высокоэнергетических топлив изоалкановые углеводороды, характеризующиеся максимальным содержанием водорода, а следовательно, максимальной весовой теплотой сгорания. Сложность заключается в "Подборе таких структур изоалканов, низкотемпературная характеристика которых (температура застывания, кристаллизации, вязкость и ее изменение с температурой) была бы удовлетворительной, а плотность максимальной.
К числу таких углеводородов относятся, по-видимому, алканы гребенчатого строения с компактно и симметрично расположенными короткими боковыми цепями, имеющими один или два углеродных атома. Предстоит изыскать наиболее экономически целесообразный путь получения алканов," отвечающих такому строению.
Известна еще одна группа углеводородов, энергоемкость которых складывается не только из теплот сгорания элементов, но и из энергии, выделяющейся при разрушении их кратных связей и напряженных циклов. К ним относятся производные ацетилена и углеводороды, в структуре которых имеются циклопропановые кольца. Энергия ацетиленовой связи -С=С- составляет около

195 ккал/моль, т. е. более чем в два раза больше энергии связи (84 ккалімоль). Однако реализовать эту дополнительную энергию весьма сложно из-за склонности ацетиленовых углеводородов полимеризоваться по месту ненасыщенных связей. При сгорании циклопропана и его гомологов также выделяется дополнительная энергия, которая в отличие от энергии ацетиленовой связи может быть использована. В табл. 21 приведены теплоты образования и сгорания некоторых углеводородов с простыми и кратными связями, а также напряженными циклами.

Как видно из данных табл. 21, циклопропан и ацетиленовые углеводороды характеризуются весьма высокими теплотами сгорания, намного превышающими теплоты сгорания насыщенных углеводородов с таким же числом углеродных атомов в молекуле, но не имеющих столь напряженных связей. Наибольшую теплоту сгорания имеет циклопропан. Гомологи циклопропана характеризуются несколько меньшей теплотой сгорания. Так, низшая весовая теплота сгорания фенилциклопропана равна 10 280 ккал/кг, циклогексилциклопропана 10 610 ккал/кг. Гомологи циклопропана имеют следующие весьма важные преимущества по сравнению с ацетиленами: хорошую стабильность при хранении, низкотемпературные свойства, невзрываемость и др.
Очевидно, ди- и трициклопропаны будут представлять собой топлива, отличающиеся наибольшей энергоемкостью среди углеводородов иного строения, в том числе алканов.
В табл. 22 приводятся значения удельных импульсов для ракетных топливных систем при использовании в качестве горючего ацетилена или циклопропана.

Циклопропилуглеводороды могут быть получены в процессе довольно сложного синтеза, проходящего в несколько стадий. Ацетиленовые углеводороды могут быть получены в известных промышленных процессах.
В отличие от циклопропанов, которые являются довольно стабильными, ацетилены нуждаются в специальных стабилизирующих добавках и с ними надо обращаться, как со взрывчатыми веществами.
Таким образом, возможность получения углеводородов с более высокой энергоемкостью нельзя считать исчерпанной.
В третьей части «Незаметных сложностей ракетной техники» я бы хотел рассказать о ещё не охваченных в первой и второй частях проблемах, которые требуют решения. Эта статья посвящена развитию темы различных ограничений, которые приводят к инженерно неоптимальным решениям.
Виды жидкого топлива
После начальных экспериментов, когда ракеты летали на этиловом спирте, азотной кислоте, скипидаре и прочих веселых веществах, самыми распространенными стали три пары ракетного топлива: кислород/керосин, кислород/водород, несимметричный диметилгидразин/азотный тетраксид. Естественно, у каждого вида топлива есть свои плюсы и минусы, которые мы сейчас и рассмотрим. Однако, сначала мне хочется дать определение удельного импульса, которое так и не прозвучало всё это время:Удельный импульс - это мера эффективности ракетного топлива. Согласно одному из определений, это количество секунд, в течение которых двигатель может развивать тягу 1 Ньютон, истратив 1 кг топлива. Удельный импульс измеряется в секундах или в метрах в секунду. УИ 1 с = 9,8066 м/с
Кислород/керосин . УИ 358 c в пустоте, усредненная плотность (плотность смеси в соотношении для работы двигателя) 1,036 г/см^3. Самое популярное топливо, самое простое в работе и самое освоенное. Главных недостатков два - не самый высокий УИ, и то, что кислород хранится в баках в жидком виде. На ракеты-носители иногда даже не ставят теплоизоляцию, и при старте с неё красиво падает намёрзший из воздуха лёд. Но для разгонных блоков теплоизоляция нужна и требует дополнительной массы. Также жидкий кислород нельзя хранить месяцами для коррекций орбиты. Есть любопытный физический хак - переохлажденный кислород, т.е. кислород при температуре ниже температуры кипения. Он чуть плотнее, поэтому в такой же бак его поместится больше, и он не так активно закипает при заправке. На этой паре летает очень много современных ракет-носителей - «Союз», «Зенит», «Атлас», «Фалькон».
Кислород/водород . УИ 455 с в пустоте, усредненная плотность 0.3155 г/см^3. Наибольший УИ, но есть серьезные недостатки. Жидкий водород доставляет гораздо больше проблем, чем кислород. Во-первых, из-за низкой плотности пары кислород/водород бак будет в 2-3 раза выше баков других топливных пар при том же диаметре. Во-вторых, бак надо делать с теплоизоляцией, потому что иначе жидкий водород будет активно испаряться. Даже с теплоизоляцией надо дренировать бак и подпитывать его жидким водородом практически до момента старта. Дренаж испарившегося водорода нужно отводить, потому что его смесь с воздухом взрывоопасна. Разгонный блок с этими компонентами должен отработать в течение нескольких минут, долгоживущие модификации блоков, которые жили часами, были изготовлены в единичных экземплярах и оказались сильно дороже. На этой паре летали шаттлы и «Энергия», летают «Дельта» американцев, «Ариан-5» европейцев и «H-II» японцев.
НДМГ/АТ . УИ 344 с в пустоте, усредненная плотность 1,185 г/см^3. УИ чуть ниже кислорода/керосина, очень высокая плотность, кипит при плюсовой температуре, самовоспламеняется при смешении компонентов, вроде бы мечта, а не топливо. Одна беда, НДМГ - жуткий яд. Высший класс токсичности по NFPA 704, мутаген, тератоген, канцероген. АТ тоже не подарок, но на класс опасности ниже, ядовит примерно как хлор, и растения после него хорошо растут - азотистое удобрение. К небольшим недостаткам этой топливной пары можно отнести коррозию материалов (но с этим можно бороться) и более высокую стоимость, чем у пары кислород/керосин. На ней летают «Протон», «Великий поход» китайцев и GSLV индусов. Летали «Титаны» американцев и «Ариан» европейцев, но в ракетах-носителях он постепенно будет сходить на нет. Опасность разлива сотен тонн компонентов при аварии и необходимость дезактивации участка падения отработанной ступени делает бесперспективным использование этой пары в ракетах-носителях. Но она используется в разгонных блоках и двигательных установках спутников, потому что может долго и без проблем храниться в полёте.
Геометрические размеры ступени, транспортировка
С точки зрения геометрии, максимальный объем при фиксированной площади достигается для шара. И аэродинамическое сопротивление и полная поверхность цилиндра пропорциональны квадрату радиуса, поэтому ракеты должны были бы быть достаточно невысокими и широкими. Однако, в реальности, ракеты очень тонкие и высокие. Дело в том, что увеличение диаметра увеличивает сложность изготовления и транспортировки ступени. У меня была гипотеза, что мера сложности работы со ступенью обратно пропорциональна квадрату радиуса. Я собрал данные о пусках ракет за последние двадцать лет (много пусков даст статистическую базу, а не очень большой временной диапазон не приведет к ошибке из-за изменения технологий) и построил график количества пусков в зависимости от наибольшего диаметра ступени (самого широкого бака). Что интересно, гипотеза подтвердилась:
Ещё можно вспомнить байку о том, как ширина двух древнеримских лошадей привела к ограничению полезной нагрузки «Спейс Шаттла». Это, конечно, байка, и даже отдел стандартизации NASA потрудился её опровергнуть , но общий принцип верен - задача транспортировки ставит большие проблемы для разработки ракет-носителей.
Кто как может
США повезло не только с широтой. Их космодром находится на берегу моря, и не составляет проблем привезти ступени на корабле или барже:
Слева баржа для транспортировки внешнего топливного бака «Спейс-Шаттла», по центру перевозка от причала в здание вертикальной сборки, справа транспорт «Дельта Маринер» перевозит ступени РН «Дельта-IV» и «Атлас- V»
Поэтому американцы могли возить ступени «Сатурна-V» диаметром 10,1 м и внешние топливные баки шаттлов восьмиметрового диаметра.
У европейцев космодром Куру тоже находится у самого берега, что опять позволяет использовать большие ступени - 5,4 м у «Ариан-5»:
Ну а у нас ситуация гораздо сложнее. Первую ступень Н-1 диаметром 17 метров сваривали уже на Байконуре, центральный блок «Энергии» возили на самолёте. Диаметр «Протона» фактически 4,1 м, боковые баки первой ступени присоединяются уже при сборке ракеты на Байконуре. И, по слухам в Интернете, при транспортировке блоков ракеты приходится перекрывать встречное движение по железной дороге. Вот он - тайный враг отечественной космонавтики - железнодорожный габарит:
Уже на вагонах «Ангары» с диаметром 2,9 м ясно виден индекс негабаритности - по ширине он почти предельный (5 из 6):
Железнодорожный транспорт для нас пока остается единственно доступным. Возить на самолёте дорого, да и ограничение размера присутствует. Новые специальные самолёты будут стоить сильно дороже. Собирать на месте очень дорого - надо новый завод строить. По рекам транспортировать тоже не получается - будут нужны специальные баржи для рек и корабли для движения по Северному морскому пути. Учитывая, что сейчас в «Роскосмосе» есть некоторое шевеление по поводу разработки сверхтяжелой ракеты, становится очень любопытно, какие геометрические параметры там выберут, и как её будут транспортировать?
Компоновка
Времена, когда денег в космос вливали много, и можно было строить такой инженерно-красивый «Сатурн-V», увы прошли. Теперь во всем мире мода на «летающие заборы» из универсальных модулей, которые должны быть удобными и дешевыми:
Слева направо: «Дельта-IV», «Атлас-V», «Фалкон-9», «Ангара»
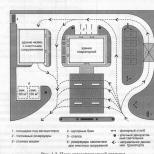
Стартовые сооружения
Меня очень занимал вопрос, чем была вызвана такая странная компоновка у «Ангары» версии 1995 года?Не нужно думать, что эту схему делали дилетанты или «враги народа». Представьте, что на дворе первая половина девяностых. На Байконуре раздрай, Казахстан, ставший независимым, может устроить проблемы с использованием космодрома. «Протон» надо чем-то заменять. Но денег у государства ни на что нет, и масштабные проекты однозначно не получатся. А на космодроме «Плесецк» есть почти достроенный старт для РН «Зенит». «Зенит» выводит на орбиту почти четырнадцать тонн. Если сделать новую ракету в размерности «Зенита», привесив дополнительные баки, то полезную нагрузку можно увеличить. Так и появилась эта странная конструкция.
Этот же фактор уже готового стартового сооружения пророчит хорошее будущее «Союзу-2.1в» . Старты для обычных «Союзов» есть на Байконуре, Плесецке, Куру (но туда вряд ли пустят - конкуренция «Веге»), строится старт на «Восточном».
Кстати, идею параллельного расположения баков реализовали ещё в «Протоне». На первой ступени стоит один бак окислителя диаметром 4,1 м. и шесть баков горючего, на которых стоят двигатели. Получилось даже изящно - на дно бака окислителя выведены коммуникации, что сделало ненужной отдельную кабель-мачту. А первая ступень стала заметно короче, что полезно для уменьшения изгибающих нагрузок и упрощает работу с ракетой в целом. Что любопытно, эту идею и сейчас не хотят забывать - вот, например, картинка неких эскизов из доклада от ноября 2013 года:

вторая слева ракета - параллельно расположенные баки на первой ступени, третья слева - боковые и центральный баки для разных компонентов
Деньги
Это ограничение фактически разлито по всем остальным, потому что любое инженерное решение имеет свою цену. Для наглядности - некрасивые ракеты на КДПВ в большинстве своем стали такими некрасивыми из-за того, что использовались уже готовые блоки разных диаметров, и увеличение диаметра спутников привело к необходимости создания надкалиберных обтекателей.
Первая слева ракета - «Тор - Эйбл». На уже существующую баллистическую ракету «Тор» поставили ступень «Эйбл», которую сделали для ракеты «Авангард».
Вторая - «Таурус». Под ступени ракеты «Пегас» воздушного старта поставили ступень с МБР «MX»
Третья - «Ариан-4». К сожалению, прямых предков я не нашёл, откуда она такая некрасивая появилась - неясно.
Четвертая - «Ариан-6». Переход на новые твердотопливные блоки, а верхняя ступень остается с «Ариан-5», поэтому она большего диаметра.
Пятая - «Ангара» версии 1995 года. О ней я уже говорил.
P.S. Из четырех последних статей две были написаны фактически по вашим заявкам. У меня есть список интересных тем, по которым можно сделать статьи, и он ещё далеко не исчерпан, но мне хочется узнать - есть ли какие-то темы, на которые вы хотели бы прочитать научно-популярную статью о космонавтике? Предлагайте свои пожелания в комментариях, если они меня заинтересуют, то я их поставлю в свою очередь статей.
Теги:
- космонавтика
- НСРТ
ЭНЕРГИЯ ТОПЛИВА
В природе существует много горючих веществ, которые при сгорании выделяют тепло.
Однако, топливом можно считать лишь те горючие вещества, у которые обладают большой удельной теплотой сгорания, низкой температурой воспламенения. отсутствием вредных продуктов сгорания, широко распространены в природе, просты в добыче и транспортировке.
Чем больше выделяется тепла при сгорании топлива, тем лучше.
Разные виды топлива одинаковой массы при полном сгорании выделяют разное
количество теплоты. Сравнить количества теплоты, выделившиеся при сгорании разных
видов топлива можно,
используя физическую величину - удельную теплоту сгорания.
Удельная тплота сгорания
показывает, какое количество теплоты выделится при полном сгорании
1 кг данного топлива.
Единица измерения
удельной теплоты сгорания в системе СИ:
[ q ] = 1 Дж/кг
Расчетная формула для количества теплоты,
выделившейся при полном
сгорании топлива:

где Q - количество выделившейся теплоты (Дж),
q - удельная теплота сгорания (Дж/кг),
m - масса сгоревшего топлива (кг).
ЗНАЕШЬ ЛИ ТЫ?
Растения ежегодно производят 300 000 000 000 т кислорода. А при старте одной лишь ракеты сжигается в качестве топлива от 100 т до 1000 т жидкого кислорода.
Можно ли получить холод при сжигании угля?

Получение из угля не жара, а холода каждодневно осуществляется
на заводах так называемого
«сухого льда».
Уголь
сжигается в котлах,
а образующейся дым очищается и содержащийся в нем углекислый
газ улавливается щелочным раствором. Затем щелочной раствор нагревают
и из него выделяется углекислый газ. Углекислый газ
при последующем
охлаждении и сжатии переводится в жидкое
состояние под давлением
70 атм. Эта жидкая углекислота в толстостенных баллонах доставляется
на заводы шипучих напитков. Она так холодна, чтобы может заморозить
грунт, как делалось при сооружении метро.
Для многих целей в промышленности и в медицине требуется углекислота
в твердом виде
– «сухой лед», который и получают при дальнейшем
охлаждении углекислоты.
Самое горячее пламя получается при сгорании субнитрида углерода (C4N2), дающего при 1 атм. температуру 5261 K.
ПЛАМЯ СВЕЧИ
В пламени любого источника света имеется очень накаленная полоса, а в других частях теплота почти незаметна. Зажгите свечу и наблюдайте за фитилем. В пламени свечи легко различить отдельные полосы. Внизу вы увидите коричневую точку l, где свет почти не воспринимаем для глаза, а несколько выше синеватую часть m.

В синюю часть пламени кислород не проникает, и газы здесь не горят, оставаясь невоспламеняемыми. Это резервуар, питающий часть n, в которой газы подвергаются полному сгоранию. Вид этой полосы ярко красный. Часть n окружает полоса r, плохо видимая , но самая горячая из всех. Здесь происходит процесс полного сжигания углерода.
Примеры
Рассмотрим пример. 10 граммов этилового спирта сгорело в спиртовке за 10 минут. Найдите мощность спиртовки.
Решение. Найдём количество теплоты, выделившееся при сгорании спирта:
Q = q*m; Q = 27 000 000 Дж/кг * 10 г = 27 000 000 Дж/кг * 0,01 кг = 270 000 Дж.
Найдём мощность спиртовки:
N = Q / t = 270 000 Дж / 10 мин = 270 000 Дж / 600 с = 450 Вт.
Рассмотрим более сложный пример. Алюминиевую кастрюлю массой m1, заполненную водой массой m2, нагрели с помощью примуса от температуры t1 до температуры t2 (00С < t1 < t2
Решение.
Найдём количество теплоты, полученное алюминием:
Q1 = c1 * m1 * (t1 t2);
найдём количество теплоты, полученное водой:
Q2 = c2 * m2 * (t1 t2);
найдём количество теплоты, полученное кастрюлей с водой:
найдём количество теплоты, отданное сгоревшим бензином:
Q4 = Q3 / k * 100 = (Q1 + Q2) / k * 100 =
(c1 * m1 * (t1 t2) + c2 * m2 * (t1 t2)) / k * 100;
найдём массу сгоревшего бензина:
m = Q4 / q = (c1 * m1 * (t1 t2) + c2 * m2 * (t1 t2)) / k * 100 / q
Ответ: масса сгоревшего бензина равна
(c1 * m1 * (t1 t2) + c2 * m2 * (t1 t2)) / k * 100 / q.
Реши самостоятельно:
Начальный уровень
1. Удельная теплота сгорания бензина 44 МДж/кг. Выберите правильное утверждение.
А. Приполном сгорании1м3 бензина выделится 44 МДж энергии.
Б. При полном сгорании 44 кг бензина выделится 1 МДж энергии.
В. При полном сгорании1кг бензина выделится 44 МДж энергии.
2. В топке было сожжено одинаковое количество каменного угля и сухих дров. Выберите правильное утверждение.
А. При сгорании каменного угля выделилось большее количество теплоты.
Б. При сгорании сухих дров выделилось большее количество теплоты.
В. При сгорании угля и дров выделилось одинаковое количество теплоты.
3. При сжигании каменного угля выделилось 54 МДж теплоты. Выберите правильное утверждение.
А. Было сожжено 1 кг угля.
Б. Было сожжено 2 кг угля.
В. Было сожжено 4 кг угля.
4. При сжигании 1 кг топлива выделилось 26 МДж теплоты. Выберите правильное утверждение.
А. Сжигали керосин.
Б. Сжигали спирт.
В. Сжигали древесный уголь.
5. Сожгли 2 кг каменного угля. Выберите правильное утверждение.
А. Чтобы выделилось такое же количество теплоты, необходимо сжечь 1,5 кг спирта.
Б. Чтобы выделилось такое же количество теплоты, необходимо сжечь 2 кг бензина.
В. Чтобы выделилось такое же количество теплоты, необходимо сжечь 4,5 кг сухих дров
6. В печи было сожжено 2 кг сухих дров. Выберите правильное утверждение.
А. Выделилось 6 МДж теплоты.
Б. Выделилось 12 МДж теплоты.
В. Выделилось 24 МДж теплоты.
Средний уровень
1. Сколько сухих дров нужно сжечь, чтобы получить 60 МДж теплоты?
2. Какое количество теплоты выделится при полном сгорании 100 г спирта?
3. При полном сгорании 0,5 кг топлива выделяется 22 МДж теплоты. Какова удельная теплота сгорания топлива? Что это за топливо?
4. Какая масса каменного угля была сожжена в печи, если при этом выделилось 60 МДж теплоты?
5. Сколько теплоты выделится при полном сгорании сухих сосновых дров объемом 3 м 3 ?
6. Сколько энергии выделится при полном сгорании керосина объемом 5 л?
Достаточный уровень
1. а) Почему порох невыгодно использовать как топливо, а бензином нельзя заменить порох в артиллерийских орудиях?
б) Сколько спирта надо сжечь, чтобы изменить температуру воды массой 2 кг от 14 °С до 50 °С, если вся теплота, выделенная спиртом, пойдет на нагревание воды?
2. а) Почему мы сильно дуем на пламя спички, свечи и т. п., когда хотим его погасить?
б) На сколько градусов Цельсия нагреются 3 кг воды, если вся теплота, выделившаяся при полном сгорании 10 г спирта, пошла на ее нагревание?
3. а) Почему рачительный хозяин предпочитает покупать березовые дрова, а не сосновые? Цена дров одинаковая.
б) Сколько дров необходимо сжечь для того, чтобы нагреть 50 л воды в железном котле массой 10 кг от 15 °С до 65 °С? Потерями тепла пренебречь.
4. а) Почему разбросанные угли костра гаснут быстро, а сложенные в кучу долго сохраняются в раскаленном виде?
б) Сколько воды, взятой при температуре 14 °С, можно нагреть до 50 °С, сжигая спирт массой 30 г и считая, что вся выделяемая при горении спирта энергия идет на нагревание воды?
5. а) Удельная теплота сгорания каменного угля примерно в два раза больше, чем удельная теплота сгорания торфа. Что это значит?
б) Сколько воды можно нагреть от 10 °С до 60 °С, если на ее нагревание пошла половина энергии, полученной в результате сгорания 40 кг каменного угля?
6. а) Почему теплота сгорания сырых дров меньше, чем у сухих той же породы?
б) На сколько изменится температура воды объемом 100 л, если считать, что вся теплота, выделяемая при сжигании древесного угля массой 0,5 кг, пойдет на нагревание воды?
Высокий уровень
1. Сколько воды можно нагреть кипятильником от 10 °С до 100 °С, сжигая в нем 0,6 кг березовых дров, если для нагревания воды пошло 25%теплоты, выделившейся при сжигании дров?
2. Сколько дров понадобится сжечь, чтобы истопить кирпичную печь? КПД печи равен 25 %, масса печи 1,5 т, в процессе протапливания температурапечи изменяется от 10 °С до 70 °С.
3. На спиртовке нагрели 175 г воды от 15 до 75 °С. Начальная масса спиртовки со спиртом была равна 163 г, а по окончании нагревания -157 г. Найдите КПД нагревательной установки.
4. В медном сосуде массой 0,5 кг нагреваются 2 л воды, взятой при температуре 10 °С. До какой температуры можно нагреть воду за счет сжигания 50 г спирта (КПД считать равным 50%)?
5. На примусе с КПД 40% необходимо вскипятить 4 л воды, начальная температура которой 20 °С, в алюминиевой кастрюле массой 2 кг. Определите расход керосина на нагревание воды и кастрюли.
6. Каково отношение масс спирта и бензина в смеси, если удельная теплота сгорания этой смеси 40 МДж/кг?